Le cœur artificiel représente une prouesse technologique et médicale majeure, ayant déjà permis de sauver de nombreuses vies. L’idée de remplacer un cœur défaillant par un dispositif médical peut sembler tout droit sortie d’un roman de science-fiction, mais il s’agit bien d’une réalité qui modifie encore aujourd’hui le paysage de la médecine cardiovasculaire. Afin de répondre à l’évolution des techniques de médecine, la collaboration des ingénieurs et des médecins a permis de développer plusieurs types de prothèses cardiaques depuis le XXème siècle.
Les premières idées
L’idée de créer un cœur artificiel s’est développée avant la seconde guerre mondiale, de par la rencontre entre Alexis Carrel, chirurgien et Charles Lindbergh, pionner américain de l’aviation. Les deux hommes ont travaillé ensemble à la création de ce cœur artificiel en 1930, qui reproduit de façon artificielle le système cœur-poumons en cherchant à maintenir en vie ces organes à l’aide d’une pompe à perfusion, surnommée le “cœur de verre”. Néanmoins les problèmes physiologiques rencontrés n’ont pas permis aux deux hommes d’aboutir.


Les premières recherches
Quelques années plus tard, en 1945, c’est au tour de Wilhem Kolff et Tetsuzo Akutsu de reprendre la réalisation de ce cœur artificiel. Pionnier du rein artificiel durant la guerre, Kolff décide de travailler avec Tetsuzo Akustu, chirurgien reconnu dans le développement de cœur artificiel, afin de créer et perfectionner cette idée. Leurs travaux reposent sur le principe d’“un cœur artificiel, qui se composerait de deux cavités ventriculaires qu’on coudrait sur les oreillettes d’un assez gros animal, un chien, par exemple. Des valves artificielles sépareraient les cavités et une membrane animée par un flux pneumatique permettrait de vider et de remplir ces cavités..”. En 1957, le cœur artificiel est né. Il a été implanté dans le thorax d’un chien, qui a survécu 90 minutes.
Les premières implantations sur l'homme
En 1963, Domingo Liotta, chirurgien argentin et ancien élève de Kolff et Akutsu , rejoint l’équipe de recherche de Michael DeBakey, père de la médecine cardiovasculaire moderne. Liotta poursuit l’idée du cœur artificiel en s’attachant à réaliser un cœur partiel, qui remplacerait uniquement le ventricule gauche. En 1966, la pompe pneumatique est implantée chez une patiente de 37 ans. 10 jours plus tard, la pompe est retirée : c’est un succès !
En 1969, Liotta travaille avec Denton Cooley à la réalisation de la première implantation totale d’un coeur artificiel (nommé Liotta-Cooley) sur un patient de 47 ans, qui décéda quelques heures plus tard d’une infection. La procédure démontrera la viabilité des cœurs artificiels comme passerelle vers la transplantation chez les patients cardiaques.
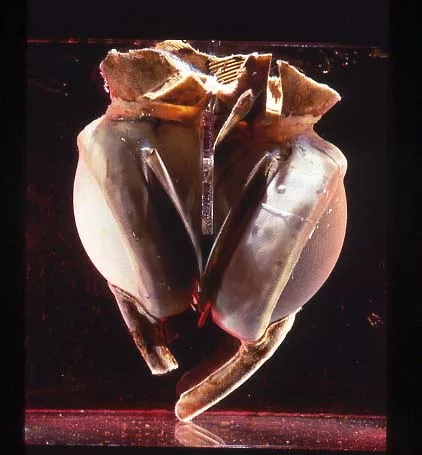

Les premiers cœurs artificiels totaux
En 1971, Robert Jarvik développe le Jarvik7, un cœur en polyuréthane, qui fut implanté chez plusieurs patients. Barney Clark, le premier patient, est resté connecté 112 jours au dispositif (dispositif qui pesait alors 180 kilos). En 2001, Abiocor I a révolutionné les prothèses cardiaques totales en supprimant tout câble (batteries implantées), mais sa taille était trop imposante pour perdurer sur le marché. En 2013, Alain Carpentier a inauguré le cœur artificiel Carmat, après plus de 20 ans de recherche, aujourd’hui commercialisé dans le cadre des études cliniques.
S’il reste encore du chemin à parcourir et que la transplantation cardiaque reste le traitement de référence, pour les patients atteints d’insuffisance cardiaques sévère, la pénurie de greffons justifie la nécessité de la conception d’un cœur artificiel de nouvelle génération comme pont à la transplantation et comme thérapie de destination. Les recherches se multiplient pour, à terme, créer le cœur artificiel qui deviendra le traitement de l’insuffisance cardiaque !
Dans cette dynamique de recherche, Procope Medicals travaille depuis 5 ans sur un prototype de coeur artificiel total en collaboration avec les chirurgiens cardiaques du CHU de Nantes. Notre objectif est d’apporter aux patients une meilleure qualité de vie, en éliminant la transmission externe avec des câbles, et en créant une prothèse disponible en 2 tailles, afin de convenir à toutes les morphologies de patients.
